JP assay data
| Crude drug latin name | BUPLEURI RADIX |
| Test name | assay |
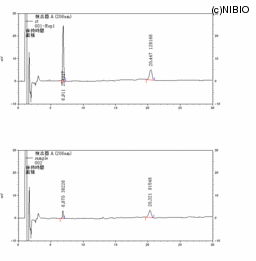
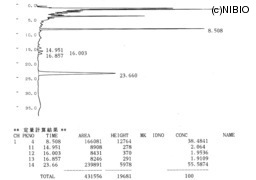
| Analytical Conditions | 本品の粉末約1gを精密に量り,共栓遠心沈殿管に入れ,薄めたメタノール(9→10)20mLを加えて15分間振り混ぜた後,遠心分離し,上澄液を分取する.残留物は,薄めたメタノール(9→10)15mLを加えて更に2回,同様に操作する.全抽出液を合わせ,薄めたメタノール(9→10)を加えて正確に50mLとする.この液5mLを正確にとり,希水酸化ナトリウム試液2.5mLを加えて50℃の水浴中で1時間加温し,サイコ定量用リン酸塩緩衝液7.5mLを加える.この液をカラム(55~105μmの前処理用オクタデシルシリル化シリカゲル0.36gを内径約10mmのクロマトグラフィー管に注入し,使用直前にメタノール10mLを流し,次に水10mLを流して調製したもの)に入れて流出させる.薄めたメタノール(7→20)10mLでカラムを洗い,次にメタノールで流出し,流出液を正確に10mLとし,試料溶液とする.別に定量用サイコサポニンa及び定量用サイコサポニンdをデシケーター(シリカゲル)で24時間乾燥し,それぞれ約10mgを精密に量り,メタノールに溶かして正確に200mLとし,標準溶液とする.試料溶液及び標準溶液20μLずつを正確に量り,次の条件で液体クロマトグラフィー〈2.01〉により試験を行う.それぞれの液のサイコサポニンaのピーク面積ATA及びASA並びにサイコサポニンdのピーク面積ATD及びASDを測定する.次式によりサイコサポニンa及びサイコサポニンdの量を求め,それらの合計を総サポニンの量とする. サイコサポニンaの量(mg)=MSA × ATA/ASA × 1/2 MSA:定量用サイコサポニンaの秤取量(mg) サイコサポニンdの量(mg)=MSD × ATD/ASD × 1/2 MSD:定量用サイコサポニンdの秤取量(mg) 試験条件 検出器:紫外吸光光度計(測定波長:206nm) カラム:内径4.6mm,長さ15cmのステンレス管に5μmの液体クロマトグラフィー用オクタデシルシリル化シリカゲルを充てんする. カラム温度:50℃付近の一定温度 移動相:水/アセトニトリル混液(3:2) 流量:サイコサポニンaの保持時間が約8分になるように調整する. システム適合性 システムの性能:標準溶液20μLにつき,上記の条件で操作するとき,サイコサポニンa,サイコサポニンdの順に溶出し,それらのピークの理論段数及びシンメトリー係数は,それぞれ4000段以上,1.4以下である. システムの再現性:標準溶液20μLにつき,上記の条件で試験を6回繰り返すとき,サイコサポニンa及びサイコサポニンdのピーク面積の相対標準偏差は,いずれも1.5%以下である. |
| Memo |
JP assay photo file
| JP assay photo file |  |
| Analytical Conditions | HPLCメーカー:島津 №2 型式:LC-20ATvPアイソクラティックシステム 使用カラム:ナカライテスク/COSMOSIL Cholester/φ4.6×150㎜ 5μm 移動相:0.05mol/Lリン酸二水素ナトリウム試液/アセトニトリル混液(5:3) |
| Memo | 原形 中国四川省 |